Emisión de Carta de Interés con Fines de Investigación
¿Qué es la Carta de Interés con fines de investigación?
La CI, también es un requisito que los investigadores deben presentar al Comité de Ética de Investigación en Seres Humanos, para la evaluación de un estudio SI este se realiza en los establecimientos y/o requiere datos.
¿Cuál es el propósito de la Carta de Interés?
A través de la CI, la institución o establecimiento público o privado puede manifestar su participación libre y voluntaria de formar parte de la investigación y además, señalar el interés y pertinencia de la utilización de datos que en esta reposen, en cumplimiento de las normativas vigentes en relación a datos.
¿Cómo solicitar la Carta de Interés? -CLIC AQUI–
La presente sección describe el procedimiento que los investigadores deben realizar para solicitar la emisión de la carta de interés con propósitos de investigación en el Ministerio de Salud Pública – MSP.
Mediante la implementación de estos procesos, el MSP busca garantizar el derecho a la protección de datos personales, así como también impulsar la
investigación ética y de calidad en el país.
https://almacenamiento.msp.gob.ec/index.php/s/CfazBYY3BrsQmAT
a. Requisitos
Para solicitar la emisión de CI con fines de investigación, el investigador principal (IP) debe presentar:
La solicitud dirigida a la máxima autoridad (formato, CLIC AQUÍ) suscrita por el IP del estudio; y, El protocolo del estudio propuesto (formato, CLIC AQUÍ).
De acuerdo al alcance (ámbito) de la investigación propuesta, el requerimiento debe dirigirse, a:
- Planta Central: Si el estudio tiene como alcance más de una coordinación zonal, o es de carácter nacional; o, si se requiere la participación de las direcciones nacionales. La solicitud debe estar dirigida a la máxima autoridad del MSP, es decir al ministro/a.
- Nivel zonal: Si el estudio abarca más de un distrito o es de carácter zonal. La solicitud debe estar dirigida a la máxima autoridad de la coordinación zonal correspondiente.
- Nivel Distrital: Si el estudio abarca el nivel territorial correspondiente al distrito, o cuando las investigaciones son propuestas en: hospitales básicos que no son entidades operativas desconcentradas y centros de salud. La solicitud debe dirigirse al director distrital correspondiente.
- Hospitales básicos que son entidades operativas desconcentradas, hospitales generales y establecimientos del tercer nivel de atención: Si el estudio tiene como alcance un determinado establecimiento de salud específico. La solicitud debe dirigirse a la máxima autoridad del establecimiento de salud correspondiente.
b. ¿Dónde solicitar la Carta de Interés?
El IP puede realizar el requerimiento:
Presencial. En ventanilla de atención al usuario en Planta Central o en los niveles desconcentrados (coordinación zonal, distrito, hospital general, hospital EOD y establecimientos de tercer nivel) del MSP; o,
En línea. A través del Sistema de Gestión Documental QUIPUX (si el solicitante cuenta con usuario en el sistema como ciudadano).
c. ¿Cuándo solicitar la Carta de Interés?
Se puede solicitar la CI, para:
- Investigaciones que requieran la participación del MSP; y/o,
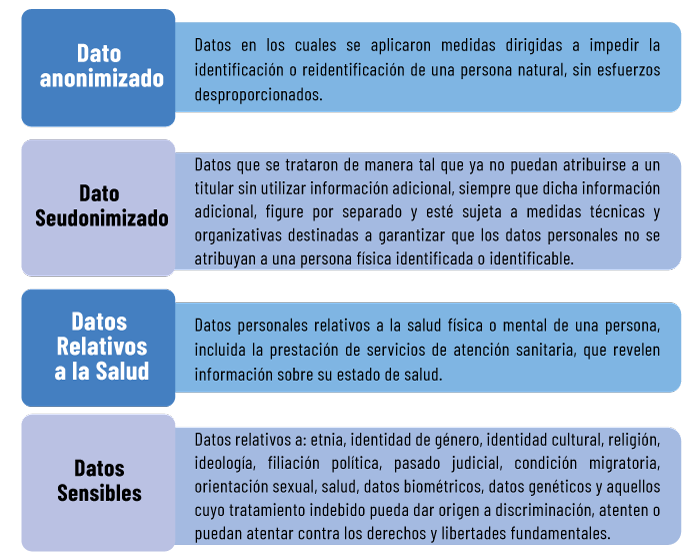
- Investigaciones que requieran la utilización de datos NO agrupados que reposan en el MSP, como:
Recordemos: Los documentos que contienen información relativa a salud son: historias clínicas, resultados de exámenes de laboratorio, imagenología y otros procedimientos, tarjetas de registro de atenciones médicas con indicación de diagnóstico y tratamientos, entre otros; siendo los datos consignados en ellos confidenciales. La autorización para el uso de los documentos antes señalados, es potestad privativa del/la usuario/a o representante legal mediante la firma del consentimiento/asentimiento informado.
¿Cómo se emite la respuesta al requerimiento?
Con la documentación presentada por el IP, el MSP realizará el análisis correspondiente y emitirá una respuesta a través del Sistema de Gestión Documental Quipux, la cual si es favorable incluirá la Carta de interés.
En el caso que la solicitud esté incompleta, se enviará una respuesta solicitando que se presente la solicitud como un nuevo trámite, donde se incluya la información requerida.
La CI debe ser presentada a un CEISH, junto con los requisitos restantes establecidos en la norma, para la evaluación del estudio.
¿Cuándo puedo ejecutar el estudio o solicitar los datos?
Con la aprobación del estudio por parte de un Comité de Ética de Investigación en Seres Humanos (CEISH) aprobado por el MSP, el investigador podrá solicitar al MSP su participación o los datos de acuerdo a señalado en la CI.
La solicitud debe estar dirigida a la Máxima Autoridad del nivel central, desconcentrado o del establecimiento de salud, quién emitió la carta de interés, adjuntado el protocolo de investigación aprobado y la carta de aprobación emitida por el CEISH. Dicha solicitud
En el caso de que el investigador requiera de talento humano o insumos de un establecimiento público sanitario para el desarrollo del proyecto de investigación, previo a la ejecución, debe suscribir un convenio según como lo determine establecimiento público sanitario, en base a lo establecido en el Acuerdo Ministerial No. 00011-2020, “Reglamento de suscripción y ejecución de convenios del MSP”, publicado en Registro oficial – Edición especial No. 590 de 20 de mayo de 2020. Cabe señalar que el proyecto de investigación previo a la suscripción del convenio deberá contar con la aprobación de un CEISH aprobado por MSP.
Base legal que sustenta el proceso
- Ley Orgánica de Salud.
- Ley Orgánica de Protección de Datos Personales
- Reglamento General de la Ley Orgánica de Protección de Datos Personales
- Políticas para el tratamiento de datos personales en el Ministerio de Salud Pública – Acuerdo Ministerial Nro. 0027-2022.
- Reglamento para la aprobación, desarrollo, vigilancia y control de investigaciones observacionales y estudios de intervención en seres humanos – Acuerdo Ministerial Nro. 0015-2021 y su reforma, Acuerdo Ministerial Nro. 0038.
- Reglamento Sustitutivo para la Aprobación y Seguimiento de Comités de Ética de Investigación en Seres Humanos (CEISH) y Comités de Ética Asistenciales para la Salud (CEAS) – Acuerdo Ministerial Nro. 0005.
- Reglamento para el Manejo de Información Confidencial en el Sistema Nacional de Salud – Acuerdo Ministerial Nro. 5216- 2015.
- Reforma al Estatuto Orgánico Sustitutivo de Gestión Organizacional por Procesos del Ministerio de Salud Pública, Acuerdo Ministerial Nro. 00023-2022.